医学研究伦理小组于2002年12月建立,成员主要由具有医学、药学、法学研究背景的人员和本单位以外的代表社区利益的非专业人士组成,男女均有,委员人数为13人。目前设主任委员1名,副主任委员1名,委员人数共13名。医学研究伦理小组的组成和工作是独立的,一切活动不受临床试验和实施者的干扰和影响。举行审查会议时至少有一名医学专业的成员,至少有一名非医学者或者非科学专业人员,至少有一名外单位的成员出席,他们均拥有投票权。
医学研究伦理小组遵守国家食品药品监督管理总局颁布的《药品临床试验质量管理规范》和《医疗器械临床试验管理规范》中的伦理审查规范,以《赫尔辛基宣言》中的伦理原则为指南。对本单位承担的以及在本单位内的实施的医学研究进行独立、称职和及时的审查。审查范围包括药物临床试验项目,医疗器械临床实验项目,涉及人的临床科研项目(包括临床流行病学研究,利用人的医疗记录和个人信息的研究,利用人的生物标本的研究)等。伦理审查类别包括初始审查、跟踪审查和复审。伦理委员会办公室负责日常行政事务的管理工作。
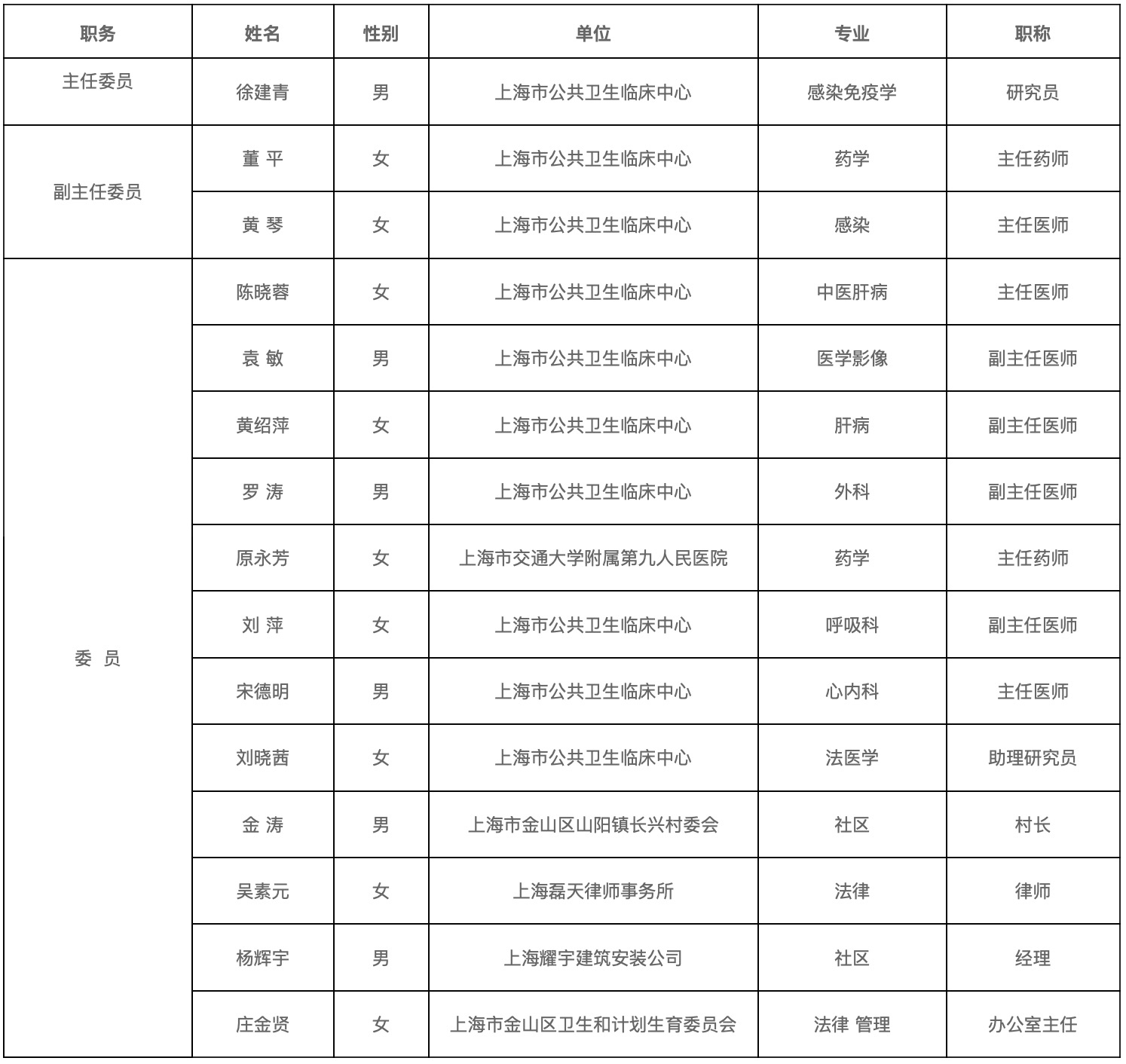
医学研究伦理小组委员名单 (2019年4月24日)